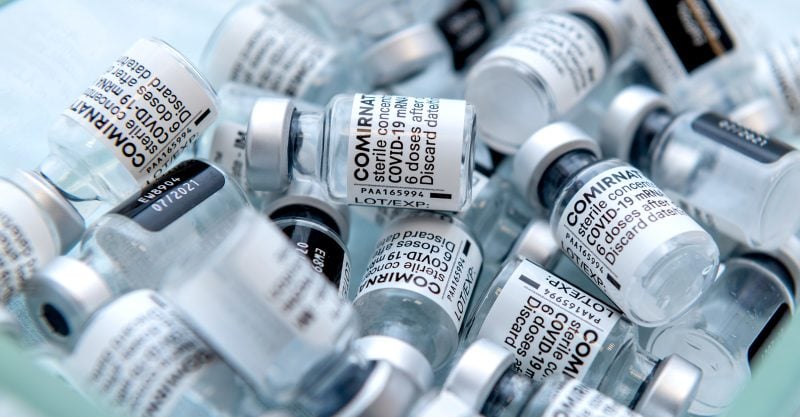
El 31 de agosto, “Children’s Health Defense” (CHD) presentó una demanda ante el Tribunal de Distrito de EE.UU., Distrito Este de Tennessee, contra la Administración de Alimentos y Medicamentos de EE.UU. (“Food and Drug Administration”, FDA por sus siglas en inglés) y su directora en funciones, la Dra. Janet Woodcock, por su presunta autorización apresurada y presuntamente engañosa de la vacuna Comirnaty de Pfizer.
CHD argumenta que la autorización fue un ejemplo del clásico truco de “ofrecer una cosa y dar otra”, que permitió a Pfizer, a la administración Biden, a los militares estadounidenses y a los empleadores exhortar a la gente a ponerse vacunas “autorizadas” cuando, de hecho, las vacunas disponibles y que se estaban administrando seguían siendo las de la Autorización de Uso de Emergencia (“Emergency Use Authorization”, EUA por sus siglas en inglés) de Pfizer-BioNTech.
Aquí está mi último con @NassMeryl… Enterrado en la letra pequeña de la aprobación del lunes por la FDA de la vacuna Pfizer Comirnaty COVID son 2 hechos críticos que afectan a si la vacuna puede ser obligatoria + si Pfizer puede ser considerado responsable de las lesiones.https://t.co/QtpHufCKDI
– Robert F. Kennedy Jr (@RobertKennedyJr) 25 de agosto de 2021
Según la demanda, la FDA violó la ley federal cuando autorizó simultáneamente la vacuna “Comirnaty” de Pfizer y extendió la EUA de Pfizer para su vacuna que tiene la “misma formulación” y que “puede usarse indistintamente”, según la FDA.
La ley(21 U.S. Code § 360bbb-3-(3)) sobre “autorización de productos médicos para uso en emergencias” exige que la designación EUA se utilice sólo cuando “no exista una alternativa adecuada, aprobada y disponible al producto para diagnosticar, prevenir o tratar dicha enfermedad o condición”.
La demanda alega que, una vez que la FDA aprobó y autorizó la vacuna Comirnaty de Pfizer, no había más base para que la FDA preservara el estatus de EUA para la vacuna de Pfizer-BioNTech que, según reconoce Pfizer, tiene la “misma formulación” y es “intercambiable”.
Según la demanda, tampoco hay base para mantener el estatus de EUA para otras vacunas COVID para el mismo uso y para la misma población que la vacuna Comirnaty de Pfizer.
“La FDA debe justificar sus acciones en un tribunal abierto”, dijo Mary Holland, presidenta y consejera general de CHD. “El lenguaje de su licencia es casi incomprensible, y el resultado de tener vacunas con y sin licencia para la misma indicación es arbitrario”.
CHD pide al tribunal que anule y detenga las decisiones de la FDA de autorizar la vacuna Comirnaty de Pfizer y de ampliar la EUA para la vacuna de Pfizer-BioNTech.
Los abogados Robert F. Barnes y Derek Jordan, de Barnes Law, son los abogados principales junto con el presidente de CHD y el asesor jurídico principal Robert F. Kennedy Jr. y otros asesores de CHD.
El 16 de mayo, CHD presentó una petición ciudadana a la FDA pidiendo a la agencia, entre otras cosas, que revoque todas las EUAs de la vacuna COVID y se abstenga de aprobar cualquier EUA futura, solicitudes de nuevos medicamentos o solicitudes de licencias biológicas para cualquier vacuna COVID para todos los grupos demográficos porque los riesgos de eventos adversos graves o muertes superan los beneficios, y porque medicamentos existentes y ya aprobados proporcionan una profilaxis y un tratamiento altamente eficaces contra el COVID, haciendo irrelevantes las EUAs. La petición obtuvo más de 30.000 comentarios públicos.
El 23 de agosto, el mismo día en que la FDA autorizó la vacuna Comirnaty de Pfizer, la agencia respondió a la petición de CHD. Esta autorización y la respuesta de la FDA despejaron la vía administrativa para que CHD presentara la demanda.