I Centri per il Controllo e la Prevenzione delle Malattie (CDC) hanno pubblicato oggi dei nuovi dati che mostrano che dal 14 dicembre 2020 al 4 novembre 2022 sono state inviate al Vaccine Adverse Event Reporting System (VAERS) un totale di 1.458.322 segnalazioni di eventi avversi in seguito ai vaccini anti COVID-19.
Il VAERS è il sistema principale, finanziato dal governo, per la segnalazione degli eventi avversi alle vaccinazioni negli Stati Uniti.
I dati comprendono un totale di 31.961 segnalazioni di decessi e 265.274 di lesioni gravi, inclusi i decessi, nello stesso periodo di tempo.
Al 4 novembre 2022 sono state registrate in totale 7.783 segnalazioni di eventi avversi in seguito al nuovo richiamo (o booster) bivalente anti COVID-19, di cui il 45% attribuite al booster di Moderna e il 55% al booster di Pfizer/BioNTech. I dati comprendono un totale di 61 morti e 434 persone lese gravemente.
Al 10 novembre, 31,4 milioni di persone hanno ricevuto la dose di richiamo bivalente aggiornata.
Dei 31.961 decessi segnalati, 20.381 casi sono attribuiti al vaccino anti COVID-19 Pfizer, 8.696 casi a Moderna, 2.773 casi a Johnson & Johnson (J&J) e nessun caso ancora segnalato per Novavax.
Escludendo le “segnalazioni estere” al VAERS, negli Stati Uniti dal 14 dicembre 2020 al 4 novembre 2022 sono stati segnalati 894.850 eventi avversi, tra cui 15.096 decessi e 93.362 lesioni gravi.
Le segnalazioni provenienti da fonti estere sono segnalazioni che le filiali estere inviano ai produttori di vaccini statunitensi. Secondo le normative della Food and Drug Administration (FDA, Agenzia federale per gli alimenti e i medicinali degli Stati Uniti) se un produttore viene informato di una segnalazione proveniente da una fonte estera che descrive una reazione avversa che non solo è grave ma non appare sull’etichettatura del prodotto, il produttore è tenuto a inviare la segnalazione al VAERS.
Dei 15.096 decessi segnalati al 4 novembre, il 7% si è verificato entro 24 ore dalla vaccinazione e il 15% entro 48 ore dalla vaccinazione.
Negli Stati Uniti, al 2 novembre erano state somministrate 640 milioni di dosi di vaccino anti COVID-19, di cui 381 milioni di dosi di Pfizer, 241 milioni di dosi di Moderna e 19 milioni di dosi di J&J.
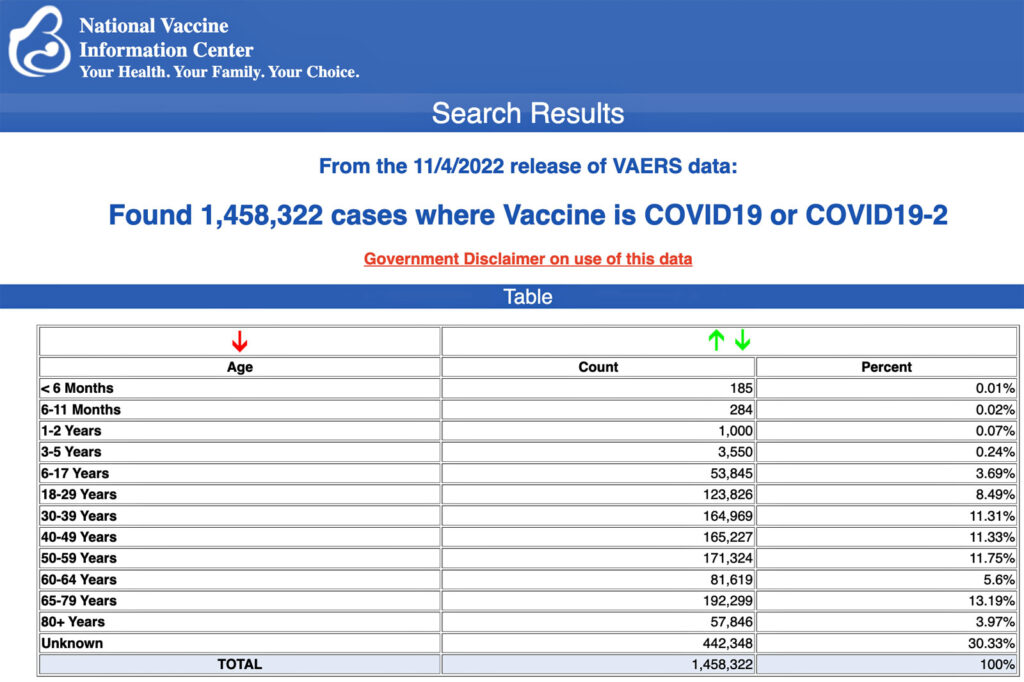
Ogni venerdì, il VAERS pubblica le segnalazioni degli eventi avversi ai vaccini a partire da una data specifica. Le segnalazioni inviate al VAERS richiedono ulteriori indagini prima che si possa confermare una relazione causale. Storicamente, è stato dimostrato che il VAERS riporta solo l’1% degli effettivi eventi avversi ai vaccini.
I dati VAERS dal 14 dicembre 2020 al 4 novembre 2022, per i bambini da 6 mesi a 5 anni, mostrano:
- 5 segnalazioni di miocardite e pericardite (infiammazione del cuore).
Il CDC usa una definizione di casistica ristretta riguardo la “miocardite”, che esclude i casi di arresto cardiaco, di ictus ischemico e di decesso dovuti a problemi cardiaci che si verificano prima che il paziente abbia la possibilità di recarsi al pronto soccorso.
- 28 segnalazioni di disturbi della coagulazione del sangue.
- 48 segnalazioni di crisi epilettiche.
I dati VAERS dal 14 dicembre 2020 al 4 novembre 2022 per i bambini di età compresa tra i 5 e gli 11 anni mostrano:
- 15.492 eventi avversi, di cui 711 classificati come gravi e 31 decessi segnalati.
- 48 segnalazioni di miocardite e pericardite.
- 72 segnalazioni di disturbi della coagulazione del sangue.
- 186 segnalazioni di crisi epilettiche.
L’ultimo decesso riportato in questa fascia d’età è quello di un bambino di 10 anni, morto improvvisamente sei giorni dopo aver ricevuto la terza dose del vaccino anti COVID-19 di Moderna. Secondo la segnalazione, “non è noto se sia stata eseguita un’autopsia”.
Secondo il commento dell’azienda (Moderna) incluso nel rapporto, “La causa del decesso è stata segnalata come arresto cardiorespiratorio. Non sono state divulgate informazioni relative alla valutazione clinica, agli esami diagnostici, al trattamento fornito o ai referti autoptici”.
I dati VAERS dal 14 dicembre 2020 al 4 novembre 2022 per i bambini tra i 12 e i 17 anni:
Secondo il CDC, “i dati VAERS disponibili al pubblico includono solo i dati della segnalazione iniziale al VAERS. I dati aggiornati, che contengono i dati delle cartelle cliniche e le correzioni apportate durante il follow-up, sono utilizzati dal governo per l’analisi. Tuttavia, per numerose ragioni, tra cui la coerenza dei dati, questi dati modificati non sono disponibili al pubblico”.
- 269 segnalazioni di anafilassi tra ragazzi di età compresa tra i 12 e i 17 anni in cui la reazione è stata pericolosa per la vita, ha richiesto un trattamento o ha causato la morte.
- 1.336 segnalazioni di miocardite e pericardite con 1.167 casi attribuiti al vaccino Pfizer.
- 303 segnalazioni di disturbi della coagulazione del sangue con 279 casi attribuiti a Pfizer.
- 27 casi di sindrome da tachicardia posturale ortostatica (POTS), tutti attribuiti al vaccino Pfizer.
I dati VAERS dal 14 dicembre 2020 al 4 novembre 2022, per tutti i gruppi di età combinati, mostrano:
- Il 16% dei decessi era legato a disturbi cardiaci.
- Il 53% dei morti era di sesso maschile, il 42% di sesso femminile e le restanti segnalazioni di decessi non riportavano il sesso del deceduto.
- L’età media alla morte era 72 anni.
- Al 4 novembre, 8.665 donne in gravidanza hanno segnalato eventi avversi correlati al vaccino anti COVID-19, tra cui 5.051 segnalazioni di aborto spontaneo o parto prematuro.
- Dei 16.634 casi di paralisi di Bell riportati, il 73% è stato attribuito alle vaccinazioni Pfizer, il 22% a Moderna e il 5% a J&J.
- 3.066 segnalazioni di sindrome di Guillain-Barré.
- 10.127 segnalazioni di anafilassi in cui la reazione è stata pericolosa per la vita, ha richiesto un trattamento o ha causato il decesso.
- 4.878 segnalazioni di infarto miocardico.
- 43.929 segnalazioni di disturbi della coagulazione del sangue. Di queste, 30.110 segnalazioni sono state attribuite a Pfizer, 9.915 segnalazioni a Moderna e 3.836 segnalazioni a J&J.
- 24.608 casi di miocardite e pericardite con 18.514 casi attribuiti a Pfizer, 5.485 casi a Moderna e 423 casi a J&J.
- 70 casi di malattia di Creutzfeldt-Jakob con 57 casi attribuiti a Pfizer, 12 casi a Moderna e 1 caso a J&J.
- 571 casi di POTS di cui 421 casi attribuiti a Pfizer, 129 casi a Moderna e 21 casi a J&J.
Children’s Health Defense (CHD) incoraggia chiunque abbia subito una reazione avversa a qualsiasi vaccino di effettuare una segnalazione seguendo questi tre punti.
Pfizer e Moderna stanno sviluppando un vaccino combinato anti Omicron-antinfluenzale a mRNA
Pfizer e Moderna stanno sviluppando un’iniezione combinata anti COVID-19 e antinfluenzale che utilizza l’mRNA che codifica per la sottovariante BA4/BA5 di Omicron e un nuovo mRNA che codifica per gli antigeni contenuti nel virus dell’influenza.
Secondo il Dr. Peter A. McCullough, poiché il componente anti COVID-19, che ha ottenuto l’autorizzazione all’uso d’emergenza (EUA), ha fallito negli studi sugli animali e non è stata riportata alcuna sperimentazione sull’uomo, questo componente dovrebbe essere escluso fin dall’inizio.
Combinare il codice genetico per la proteina spike del SARS-CoV-2 e per le proteine conservate dell’influenza A e B significherebbe installare il codice genetico di lunga durata per più proteine estranee nel corpo umano.
La produzione di queste proteine indurrà una risposta immunitaria continua e multiforme che potrebbe creare effetti collaterali amplificati. L’mRNA codificante per l’influenza sarebbe un nuovo prodotto biofarmacologico non sottoposto ad EUA e dovrebbe passare attraverso l’intero ciclo quinquennale di sviluppo normativo per i biofarmaci genetici.
Tuttavia, sembra che le aziende produttrici di vaccini stiano cercando di abbreviare questo ciclo di sviluppo combinando il vaccino antinfluenzale non di emergenza con il vaccino anti COVID-19 sotto EUA.
Il comunicato stampa della Pfizer sul nuovo booster bivalente suscita interrogativi
Il 4 novembre, Pfizer ha annunciato quelle che alcuni media hanno definito “buone notizie” sul suo booster bivalente anti COVID-19, per il quale la FDA in agosto ha concesso l’EUA sulla base di test condotti su otto topi.
In un comunicato stampa, Pfizer ha riassunto i dati aggiornati dello studio clinico di fase 2/3 sul vaccino bivalente anti COVID-19 adattato a Omicron BA.4/BA.5 di Pfizer-BioNTech.
Nei termini più semplici possibili, il richiamo bivalente ha aumentato gli anticorpi contro le sottovarianti di Omicron di 13,2 volte, mentre il richiamo originale li ha aumentati solo di 2,9 volte. L’aumento è stato riscontrato solo nelle persone di età superiore ai 55 anni.
Sebbene il nuovo richiamo abbia prodotto un aumento più modesto (9,5 volte) degli anticorpi nel gruppo di età più giovane (18-55 anni), Pfizer ha scelto di non riferire quale fosse la risposta nel gruppo di età corrispondente che aveva ricevuto il richiamo originale.
Pfizer non ha fornito alcun risultato comparativo nel gruppo 18-55 anni e nessuna differenza di esito clinico in termini di infezioni da COVID-19, né nel comunicato stampa del 4 novembre né in un precedente comunicato stampa sempre di Pfizer che riassumeva i dati preliminari.
A che punto un “aumento della risposta anticorpale neutralizzante” conferisce una “protezione più forte”?
Né BioNTech, che ha coprodotto il vaccino anti COVID-19 di Pfizer/BioNTech, né l’FDA lo sanno – nonostante insistano nel dire che l’agenzia ha motivi sufficienti per convincere/spingere/costringere coloro che hanno acquisito gli anticorpi della SARS-CoV-2 da un precedente incontro con il virus della COVID-19 a vaccinarsi comunque.
Rutgers annuncia la sperimentazione del vaccino anti COVID con Pfizer, mentre la causa di CHD contro Rutgers va avanti
Il 7 novembre, CHD ha presentato una sintesi del suo ricorso in una causa contro la Rutgers University per l’obbligo vaccinale anti COVID-19 da parte dell’università.
L’avvocato che rappresenta CHD e 13 studenti della Rutgers University nella causa ha affermato che la Corte distrettuale del New Jersey non ha seguito gli standard legali quando ha archiviato il caso di CHD.
In un’intervista rilasciata questa settimana a The DefenderJulio C. Gomez di Gomez LLC, avvocato principale della causa, ha dichiarato che l’argomentazione con cui il giudice distrettuale statunitense Zahid N. Quraishi ha accolto la mozione di archiviazione dell’università “non ha accettato i fatti riportati nella denuncia dei querelanti come veritieri”, come richiesto dagli standard legali sulle mozioni da archiviare.
Il 19 ottobre CHD ha impugnato la decisione e il 7 novembre ha presentato una sintesi del ricorso.
Gomez ha anche parlato con The Defender dell’annuncio della Rutgers University, il 4 novembre, di una collaborazione con la Pfizer per un nuovo studio clinico volto a valutare la sicurezza e l’efficacia del vaccino bivalente anti COVID-19 nei bambini di età inferiore ai 5 anni.
Il nuovo studio clinico è un’ulteriore prova dei conflitti di interesse della Rutgers in relazione alle politiche sul vaccino anti COVID-19, ha dichiarato Gomez.